Mutasyonlar, canlı çeşitliliğinin en önemli kaynaklarından birisidir. Evrim karşıtlarının sıklıkla öne sürdüğü iddia, bütün mutasyonların zararlı, dolayısıyla da canlıyı deforme eden, geliştirmeyen veya ona herhangi bir faydalı özellik katmayan anomaliler olduklarıdır. Bu iddia her ne kadar bilimsellikten uzak da olsa, kafalardaki soru kabaca anlaşılmaktadır ve bu yazının amacı da o soruya cevap vermektir.
Öncelikle bütün mutasyonların zararlı olduğuna ilişkin bilgi hatasını düzeltmek gerekiyor: Genlerde meydana gelen mutasyonlar, faydalı, etkisiz veya zararlı olabilir. Örneğin, E. coli bakterilerinde günde yaklaşık 10 milyon, insanda günde yaklaşık 10.000 mutasyon meydana gelmektedir. Çoğu mutasyon zararlı değil, etkisizdir. Nachman ve Crowell, insanlarda nesil başına yaklaşık 175 mutasyondan sadece 3’ünün zararlı olduğunu öngörmüştür. Belirgin etkileri olanların çoğu zararlıdır, ama faydalı olanların oranı da evrim karşıtlarınca öne sürülenden çok daha fazladır. Popülasyona yeni zararlı mutasyonlar eklendikçe; doğal seçilim, mevcut zararlı özellikleri ortadan kaldırır. Değişen bir ortamda faydalı bir mutasyon meydana geldiği zaman, genellikle popülasyonda hızla yayılır (Elena et al. 1996). Bu nedenle zararlı mutasyonlar uzun süre dayanamaz; faydalı mutasyonlar ise çok daha kalıcıdır.
Fakat mutasyonlar, canlının ihtiyaçlarını karşılamaya çalışmazlar. Yani bir mutasyonun gerçekleşip gerçekleşmemesi, o mutasyonun organizma için yararlı olup olmamasına bağlı değildir. Ayrıca mutasyonlar başlangıçta zararlı bile olsalar, evrimsel süreçte yarara dönüşebilir ya da bir ortamda zararlıyken, başka bir ortamda yararlı bir durum yaratabilirler.
Her mutasyon evrime yol açmaz ve yine her mutasyon evrim için önemli değildir. Örneğin otozomal hücrelerde meydana gelen mutasyonlar (yani bedensel mutasyonlar) sonraki nesillere aktarılmaz, çünkü sadece eşey hücrelerindeki kalıtsal malzeme sonraki nesle aktarılabilir.
Bir diğer önemli nokta da şudur: Mutasyonlar evrimde rol oynayan tek mekanizma değildir. Yani evrim, mutasyonlardan ibaret değildir. Ama mutasyonlar, popülasyonlara çeşitlilik ekleyen tek doğal süreçtir. Seçilim ve genetik sürüklenme ise çeşitliliği ortadan kaldırır. Doğal seçilim, çevreyle ilgili bilginin, canlının genomuna; dolayısıyla da canlının kendisine iletilmesini sağlayan süreçtir (Adami et al. 2000). Doğal seçilim, uyarlı olmayan çeşitliliği önleyerek, canlıya çevresiyle ilgili bilgi aktarır ve onun çevresine daha uyumlu hale gelmesini sağlar. Mutasyonlar yeni çeşitlilik yaratmıyor olsaydı, şu anda seçilimin etki edeceği bir çeşitlilik de olmazdı. Yani doğal seçilim zaten, mutasyonların popülasyonlara eklemiş olduğu rastgele çeşitlilik üzerinde oluşur. (Biyologlar bugün mutasyonların, değişimin ana motoru olmayabileceğini biliyor. DNA, genleri açıp-kapatan proteinler tarafından da değiştirilebilir. Bu işleme cis-regülasyonu denir. Bir de epigenetik adı verilen yeni ve dev bir çalışma alanı var. Bu iki kavram Darwin'in, genlerin orada öylece pasif bir şekilde duarak, çevre şartlarına göre değiştikleri yönündeki varsayımını çarpıcı şekilde değiştirir. Çok basitçe ifade etmek gerekirse; biyologlar DNA'nın doğal olarak seçilen özellikleri ilerletebildiğini keşfetmiştir.)
Bir diğer önemli nokta da mutasyonların rastgele ve rastlantısal olmasıdır. Bu nedenle evrimi sadece mutasyonlardan ibaret sananların, evrimi de şans eseri veya tesadüfen meydana gelen bir süreç şeklinde algılamaları doğaldır. Ancak doğal seçilim, şansın tam tersidir. Mutasyonların rastlantısallığı ile ilgili okunması gereken kısa bir yazı için tıklayın.
Burada basit ama bir o kadar da önemli bir ayrımı yapmak gerekiyor: Bir mutasyonun “faydalı” olması, mutasyonun gerçekleştiği genin sahibi olan canlı için kullanılan bir kavramdır. Yani o canlıdaki mutasyonun “insana” faydalı olmasından bahsedilmemektedir. Örneğin insan genlerindeki bir mutasyon, eğer insan için faydalıysa, faydalı bir mutasyondur; aynı şekilde, örneğin bir bakteride meydana gelen mutasyon bakterinin yaşamını iyileştiriyorsa, faydalı bir mutasyondur. Bakteride meydana gelen faydalı bir mutasyon bakterinin üremesini kolaylaştırdığı için insana zararlı olabilir, ama bundan dolayı ona zararlı mutasyon denmez. Yani gerçekleştiği canlıya göre fayda-zarar ilişkisi gözetilir. Bu konuda bile kafa karışıklığı ve çarpıtma olabildiği için özellikle belirtmek istedim.
Bazı faydalı mutasyonlar:
1. CCR5 genindeki mutasyon HIV'den AIDS'e geçişi yavaşlatır ve aynı gende gerçekleşen iki mutasyon, bir kimsenin HIV enfeksiyonuna karşı direncini arttırır
Bugün, büyük bir evrim deneyinin içinde yaşıyoruz. Gözlerimizin önünde evrim geçirmekte olan ve AIDS hastalığına neden olan HIV salgını..HIV denilen virüs, 19. yüzyılda bilinmeyen, ancak şimdi çok tanıdık hale gelen bir organizma.
Evrim karşıtları için bile, HIV, değişerek üremenin kanıtıdır, çünkü bu sürecin gerçekleşmesine tanık oluyorlar. Kısacık geçmişinde virüsün yapısı değişim gösterdi ve karşılaştığı yeni durumlara karşı uyum sağlamayı başardı. Ölüm yaklaştığında hasta, kendisini enfekte etmiş virüsten, insanla kuyruksuz maymunlar arasındaki fark kadar değişiklik gösterebilen, virüsün torunlarının yuvası olmuştur artık. Bu sitede, HIV virüsünün kendisinin geçirdiği evrimle ilgili ayrıca yayınlanmış bir yazı bulacaksınız, ama buradaki konumuz insanda meydana gelen faydalı bir mutasyon olduğu için, virüsün doğasına burda girmeyeceğiz. HIV virüsünün geçirdiği evrimle ilgilenenler buradan detaylı bir yazıya ulaşabilirler.
Konumuz insandaki bir genin uğradığı mutasyondur. C-C kemokin reseptör5 (CCR5), insanlarda CCR5 geniyle kodlanmış bir proteindir. CCR5, baskın olarak T hücrelerinde, makrofajlarda, dendritik hücrelerde ve mikrogliada etki gösterir. Bu genin insandaki enflamatuar cevapta rol oynadığı düşünülmektedir.
Bazı popülasyonlar, Delta32 mutasyonunu kazanmıştır ki bu mutasyon CCR5 genindeki genetik bilginin bir kısmının silinmesine sebep olmuştur (32-bp segment silinmesi). Bu mutasyonu taşıyan homozigot bireyler, HIV enfeksiyonuna karşı tamamen ya da kısmen dirençlidir.(yukarda söylediğimiz gibi, homo-heterozigot olmasına göre değişir.)
HIV, saldıracağı hücrelere girmek için bir ön reseptör olarak çoğunlukla CCR5 veya CXCR4’i kullanır. Delta32 mutasyonu ile, reseptör çalışamaz hale geldiği için HIV virüsünün tutunması ve hücreye girmesi engellenir, bu alel genlerden 2 kopya olması , HIV için daha da yüksek bir direnç oluşturur.Bu aleller, Avrupalılarda %5-14 oranında bulunur, Afrika ve Asya’da ise nadirdir.Birçok çalışma, bu alellerden sadece birinin varlığının bile, HIV taşıyıcısı kişilerde AİDS hastalığının oluşmasını 2 yıl geciktirdiğini göstermektedir.
2. Klamidya ve karanlığa uyum
Klamidyalar, ışıkta fotosentez yapabilen ama karanlıkta da karbon kaynağı olarak asetatı kullanarak az da olsa bir süreliğine büyüyebilen bir tür tek hücreli yeşil alg türüdür. Graham Bell, klamidyaları karanlık ortamda yüzlerce nesil üretmeyi başardı ve şöyle bi sonuç elde etti: Deneyin ilk başında bazı klamidyalar karanlıkta gayet iyi büyürken, bazıları hiç büyüme göstermemişti. 600 jenerasyon sonra ise, klamidyaların büyük çoğunluğu karanlıkta gayet iyi büyüyebilir hale gelmişti. Popülasyonun hemen hepsi, karanlıkta yaşamaya uygun hale getiren mutantlardan oluşuyoru.Bu deney, faydalı mutasyonların popülasyondaki dağılımının, hayatta kalmak için ışığa nerdeyse bağımlı olan bir canlıda ne kadar hızlı arttığını ve sonunda canlının ışıksız ortamda sorunsuzca yaşayabilir hale geldiğini göstermesi açısından önemlidir.
3. Domuz gribi virüsü H1N1′in geçirdiği mutasyon
California Teknoloji Enstitüsü’nden -Nobel ödüllü- Prof. David Baltimore ve ekibi, domuz gribi virüsünün yayılmasını sağlayan bir mutasyonu tanımladı ve Science dergisinde yayınladı. Domuz gribi virüsü diye bilinen H1N1′in bazı örneklerinin zaten yararlı bir mutasyon taşıdığı biliniyordu. Bu mutasyon, virüsün, çoğalmasını engelleyen bir ilaca (oseltamivir, piyasa ismi Tamiflu) karşı bağışıklık kazanmasını sağlıyor, ama yan etki olarak virüsün yayılmasını yavaşlatıyordu. Bu nedenle de fazla yayılamıyor ve pek de ciddi bir sağlık sorununa dönüşecekmiş gibi durmuyordu.
Ancak 2007-2008 sezonundaki domuz gribi, hem dirençliydi, hem de hızla yayıldı. Yavaş olması beklenen dirençli virüs nasıl olup da bu kadar hızlanmıştı? Antibiyotik direncini sağlayan mutasyona ek olarak bu virüsler, iki ayrı mutasyon daha geçirmişler, ve hızla çoğalma yeteneğini kazanmışlardı.
Bu iki yararlı mutasyon, dirençsiz bir virüste birbiri ardına meydana gelmiş ve direnç kazandıran mutasyonun yavaşlatıcı etkisini baştan azaltmıştı. Böylelikle bunun ardından meydana gelen direnç kazandırıcı mutasyon bir zarar vermeden canlıya yarar sağlamıştı. Bu üç mutasyon, virüse o kadar yarar sağladı ki virüs tüm dünyaya kısa sürede yayıldı.
4. Klebsiella aerogenes bakterisi ve fucose isomeraz enzimi
Robert Mortlock, Klebsiella aerogenes bakterisinin mutasyon geçirerek, daha önce bünyesinde sürekli üretilmeyen bir enzimi (fucose isomeraz) sürekli üretmeye başladığını bulmuştur. Her daim kullanılmayan bu enzimin, sürekli olarak üretilmesine yönelik bu mutasyon, zararlı gibi görünmektedir çünkü bakteri için enerji ve kaynak israfıdır. Ancak bu enzimin her an vücutta bulunmasıyla Klebsiella aerogenes bakterisi, daha önce aralıklarla metabolize edebildiği besinleri, her an kullanabilir hale gelmiştir. Dolayısıyla başlangıçta zararlı bir mutasyon olarak ortaya çıkan durum, sonunda faydalı hale gelmiştir.
5. Bakterilerdeki antibiyotik direnci
Bilindiği üzere, sürekli ve düzensiz antibiyotik kullanımı, bakterilerde bir süre sonra o antibiyotiğe karşı direnç gelişmesine sebep olur. Çoğu zaman, mutasyon sonucu gelişen bu direnç, bakterinin antibiyotiksiz ortamda yaşamasını zorlaştırıcı bir durum da yaratır. Dirençli bakteriler, antibiyoktiksiz ortamda mutasyona uğramamış olanlara göre daha yavaş ve zor ürer. Yani direnç gelişimi, antibiyotiksiz ortamda bakterinin üremesi ve çoğalması adına zararlı bir mutasyon olsa da; insan vücuduna, yani antibiyotikli ortama giren aynı bakteri için faydalı bir durumdur.
Bakterilerin antibiyotik direnci kazanmasının farklı genetik mekanizmaları vardır:
• Kromozomda oluşacak bir mutasyon, en sık rastlananlardan biridir. Mesela bakterinin hücre duvarında yer alan proteinin geninde meydana gelen mutasyon, antibiyotiin bu proteine bağlanmasına ve etkisini göstermesine engel olur. Proteinin işlevine bir zararı olmayan bu mutasyon, onu antibiyotikten koruyarak bakteriye yaşamsal değeri olan bir katkı yapmış olur.
• Kimi bakteriler ise daha önceden sahip oldukları direnç genlerini, antibiyotiğin varlığında harekete geçirirler. Bu genler, genelde bakterilerin içinde yuvarlak DNA halkaları olan plazmid yapılarında taşınır ve bu plazmidlerin diğer bakterilere aktarımı, bakteri dünyasında olağandır.
• Virüsler, bu direnç genlerini bakteri genomuna sokabilir.
Antibiyotik direncinin gelişmesi, mükemmel bir doğal seçilim örneğidir. İlaçların aşırı yaygın ve kontrolsüz kullanımı (örneğin, her burun akıntısında antibiyotiğe sarılmak) hassas bakterileri öldürürken, az sayıdaki dirençli bakterinin hayatta kalmasına ve zamanla bakteri popülasyonunda bu dirençli bakteri nüfusunun artmasına sebep olur. Yapılan çalışmalarda görülmüştür ki, bakteriler eninde sonunda her antibiyotiğe direnç geliştirir (Neu, 10992). Bir bakteride evrilen bu direnç, genetik mekanizmalar sayesinde hızla diğer bakterilere de yayılır.
Sadece terimlerle ilgili karmaşadan yola çıkarak ve sözcük oyunları yaparak bu süreçlere başka anlamlar yüklemeye çalışmak, Bu kısmı ben ekledim: toplum sağlığını ilgilendiren böylesine önemli bir tıbbi konuda insanları yanlış yönlendirmekten başka bir şey değildir. Bugün bildiklerimiz ve hastalıklarla savaşmamızda bize yol gösteren en önemli veriler, evrim kuramından gelmektedir. Bakteriler her geçen gün yeni geliştirilen ilaçlara da direnç geliştirmektedir. Dirençli bakteriler konjugasyon yoluyla yeni kazandıkları direnç genlerini diğer bakterilere de aktarabilirler. Bulaştırıcı ve öldürücü özelliklerinden dolayı bu antibiyotik dirençli organizmalar, süper bakteriler (çok sayıda ilaca dirençli [MDR] bakteriler) olarak adlandırılırlar. Hastalıklarla mücadeledeki başarımız, evrim mekanizmaları hakkında bildiklerimize ve bu konuda yapılacak olan yeni keşiflere bağlıdır. Antibiyotik direnciyle ilgili burada alıntı yaptığım yazının tamamını okumak için tıklayın.
6. Drosophila'da kanatların büyümesini durduran mutasyonlar
Bu mutasyonlar, sineğin şiddetli rüzgarlar bulunan adalarda sağ kalma yeteneğini geliştirmekte ve mutant bireyler için faydalı hale gelmektedir.
7. Sitrik asit tüketmeye başlayan bakteriler
Prof. Richard Lenski’nin, laboratuvarda gözlenmiş bir mutasyonu tarif eden “uzun vadeli evrim" deneyi için tıklayın. Bu deneyde, özetle, başlangıçta ortamdaki sitrik asiti enerji kaynağı olarak kullanamayan bakteriler, hiçbir müdahale altında kalmadan, kendiliğinden mutasyon geçirerek bu maddeden istifade edebilir hale geldi. Bu deney 1988 yılında, 12 özdeş Escherischia coli (koli basili) ekiniyle başlatıldı. Yani bakteri, deney boyunca bir deney tüpünün içinde kendisine uygun bir ortamda yetiştirildi. Her gün (yani 6-7 nesilde bir), eldeki bakterilerin %10'u yeni bir tüpe aktarılırken, geri kalan %90'ı çöpe atıldı. Yalnız her 500 nesilde bir, normalde çöpe gidecek bu %90'lık kısım derin dondurucuya kondu. Bakterileri donuk şekilde saklamak, gerektiğinde çözüp üzerinde tahlil yapmak mümkün olduğundan, bakterilerin zaman içinde bir arşivi tutulmuş oldu. Deney boyunca bu bakteriler, içinde az miktarda glukoz ve bol miktarda sitrik asit bulunan sıvı ortamda yetiştirildiler, ancak sitrik asiti kullanma imkânları olmadığından yalnızca glukozla idare ettiler. Ne var ki 33.127 nesil sonra tüplerin birindeki bakterilerin birden bire sitrik asiti kullanmaya başladıkları fark edildi. Bunun üzerine araştırmacılar donuk bakteri arşivlerini açıp önceki nesillerden bakterileri inceleyince gördüler ki sitrik asiti kullanabilen bakteriler yaklaşık 31.500. nesilde ortaya çıkmış, ve sayıları biraz dalgalanıp 33127. nesilde patlamıştı. Bu dalgalanmaları, bu bakterilerde tek bir mutasyonun değil, birden çok mutasyonun bu yeni beceriyi sağladığına yoruyorlar.
Bakterilerin yaşadığı fiziksel şartlar deney boyunca sabit olduğundan ve bu bakterilere yatay gen aktarımını engellemek için hareketli genlerden arındırılmış ortamlar kullanıldığından, bu sitrik asit kullanma becerisinin kendiliğinden meydana gelen mutasyonlara bağlı olduğundan eminler. Lenski ve meslektaşları şimdi bu sitrik asiti kullanma becerisinin tam olarak hangi genlerdeki mutasyonlara bağlı olduğunu ve bu genlerin hangi hücresel düzenekler yoluyla yarar sağladığını araştırıyorlar.
8. Bulundukları zeminin rengine uyum sağlayan fareler

Şekil 1. Hoekstra ve ekibi, aynı türden ama farklı renk tüy taşıyan farelerdeki yararlı değişinimi tanımladı. Bu fotoğrafta fareler doğadakine zıt zemin üzerinde görülüyor. (Fotoğraf: Emily Key)
Araştırma, ABD’deki bir kumulda ve etrafındaki toprak bölgede yaşayan fareler (Peromyscus maniculatus) üzerinde yapıldı . Bu farelerden, açık renkli kumul üzerinde yaşayanların açık renkli tüylere, koyu renkli topraklarda yaşayanların ise koyu renkli tüylere sahip olduğunu gören Dr. Hopi Hoekstra ve meslektaşları, bu durumun farelerin yırtıcı kuşlardan gizlenmelerini sağladığını ve dolayısıyla bu uyumun yararlı bir mutasyonun ürünü olduğunu öngördüler. Bunu sınamak için bu farelerin kalıtım bilgisini incelediklerinde, bu uyumdan tek bir gendeki (Agouti) mutasyonun sorumlu olduğunu buldular. Yaptıkları topluluk kalıtımı hesaplamaları bu mutasyonun bundan 4.000 yıl önce meydana geldiğini gösterdiği için, ve yerbilimsel çalışmalar bu coğrafi bölgenin 8.000-10.000 yıl önce oluştuğunu gösterdiği için, bu mutasyonun farelerin buraya göç etmesinden sonra meydana geldiği sonucuna vardılar.
Hoekstra ve ekibi bu mutasyonun etki şeklini de açıklığa kavuşturdu: Mutasyon, genin protein kodlayan kısmında değil, o proteinden ne kadar üretileceğini belirleyen kısmında meydana geldi. Yani fare aslında tamamen aynı proteinleri üretiyor ama daha fazla ürettiği için koyu renkli pigment (tüylere rengini veren madde) azalıyor ve tüyler daha açık renkli oluyor. Hoekstra’nın öğrencileri şimdi bu değişimlerin DNA’nın tam olarak neresinde meydana geldiğini bulmaya çalışıyor.
9. Lucilia cuprina türü sineklerin zehire karşı dirençleri
Lucilia cuprina türü sineklerin, zehire karşı dirençleri, bir nokta mutasyonuna bağlıdır. Bu zehir, asetilkolinesteraz adlı enzimi hedef alır, ona bağlanır ve onu görevini yerine getirmekten alıkoyar. Asetilkolinesteraz enziminin bu sinekteki karşılığı E3 üzerinde çalışan araştırmacılar, bu enzimden sorumlu olan geni incelediklerinde, beş ayrı nokta mutasyonu saptadılar. Bunlardan hangisinin veya hangilerinin bu dirençten sorumlu olduğunu araştırırken, ipucu, aynı direnci gösteren başka bir sinek türünden (Torpedo californica) geldi: Bu sinekler aynı direnci, bu beş mutasyondan yalnızca biri ile elde etmişlerdi. Ayrıca, ancak bu mutasyonla etkilenen amino asit, enzimin işlevini değiştirebilecek bir noktada yer alıyordu. Bunun üzerine araştırmacılar bu mutasyonlarla meydana gelen enzimlerden hangisinin organofosfatları parçalayabileceğini incelediler ve öngördükleri sonucu elde ettiler: Enzimin 137’nci amino asiti glisinden aspartik asite dönüşmüş, bu da GGT diziliminin GAT’ye dönüşmesiyle olmuştu . Ve bu mutasyon, bu enzime, kendini etkisizleştiren zehiri parçalama özelliği kazandırmıştı. Yani tek bir bazın değişimi, bu sinekleri ölümden kurtarmıştı.
10. Akdeniz Kansızlığı (=Thalasemi, AK) ve sıtmaya yakalanmayan bireyler
Bir kromozomda belirli bir genin iki kopyası (alel) bulunur. Akdeniz kansızlığı hastalığı, ilgili genin her iki aleli de mutasyon gerirmişse meydana gelir. Bu kişilerde alyuvarlardaki hemoglobin molekülü görevini yerine getiremez.
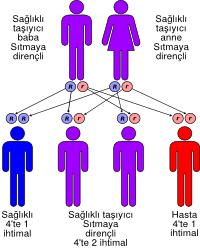
Şekil 2. Akdeniz kansızlığı geninin iki kopyasını taşıyan (kırmızı) bireyler bu hastalığa yakalanırken, tek kopyasını taşıyan (mor) bireyler Akdeniz kansızlığına yakalanmadan sıtma hastalığına karşı direnç kazanırlar.
Bir mutasyona uğramış, bir normal alel taşıyan bireylerse AK’na yakalanmadıkları gibi, sıtma hastalığına karşı başka insanlarda görülmeyen bir direnç kazanırlar. Peki bu direnç nasıl oluşur? Bazı uzmanlar, AK genini taşıyan bireylerde sıtma mikrobunun ya daha az çoğalma fırsatı bulduğunu ya da içinde yuvalandıkları arızalı alyuvarların dalakta parçalanmasıyla öldürüldüklerini düşünüyorlar. Bunun nasıl olduğuna henüz kesin bir açıklama getirilmemiş olsa bile, bu mutasyonun yararlı etkisi ortada: Sıtmanın çok görüldüğü bölgelerdeki AK oranının, sıtmanın görülmediği bölgelere göre yüksek olduğu biliniyor. Belli ki sıtmaya yakalanmaktan koruyan bir gen, belirli şartlarda zararlı olmasına rağmen, sıtma karşısında yarar sağladığı için o canlıda barınabiliyor.
11. Naylon lineer oligomer hidrolaz enzimi
Konuyla ilgili yazıya ulaşmak için tıklayın.
12. Çıplak kör farenin ölen genleri
Doğu Afrika'nın kurak bölgelerinde yaşayan çıplak kör fareler (Heterocephalus glaber) tamamen tüysüz, 10 cm. boyunda, Kemirgenler takımına ait hayvanlardır. Dişleriyle açtıkları yer altı tünellerinde yaşar, çoğunlukla kök yerler. Yer altında karanlıkta yaşadıkları için çıplak kör farelerin görme yetileri evrimsel süreçte körelmiştir; tıpkı köstebekler ve Anadolu ve Ortadoğu'da yaygın bir tarım zararlısı olan kör fareler gibi.
Çıplak kör farenin genomu ve transkriptomu Ekim 2011 tarihinde Nature dergisinde yayımlandı. Sonuçlar, bu ilginç hayvanın genetik evrimine ve kimi özelliklerini nasıl kaybettiğine ışık tutuyor. Genom dizisi, çıplak kör farenin fare ve sıçandan 73 milyon yıl önce ayrıştığını gösterdi. Kemirgenler ve -insan dahil- primatların ise 93 milyon yıl önce ayrıştığı bilinmekte. Yani çıplak kör fare, kemirgen takımından da olsa, farelerin ancak çok uzak bir akrabası.

Fotoğrafta, çıplak kör fare görülmektedir.
Çözümlemenin asıl ilginç kısmıysa çıplak kör fare genomundaki işlevini yitiren, kısaca ölen genlerdi. Genlerin işleyişlerine dair bilgi dağarcığımızı kullanarak, bir canlının hangi genlerinin artık işlevini yitirdiğini bulabiliriz. Örneğin o genin DNA dizisini silen veya proteine bağlanma yeteneğini bozan bir mutasyon gerçekleşirse, gen artık protein üretemez hale gelir, bir diğer deyişle ölür. Eğer genin canlı için önemi kalmamışsa, mutasyonların da zararı kalmaz, hattâ faydalı bile olabilirler.
Çıplak kör farenin genomunda da bu şekilde 'ölen' genlerin, artık kullanılmayan işlevlere ait olduğu bulundu. Örneğin ölen genler arasında görme ve üremeyle ilgili genler öne çıkıyordu. Bu değişimlerin, kör farelerin karanlıkta görsel duyularını kullanmamaları, öte yandan koloni yaşamında cinsel rekabetin ortadan kalkmasıyla ilgili olduğunu tahmin etmek zor değil. Keza görme, vücut ısınması ve acı hissiyle ilgili kimi temel genlerde, işlevlerini bozması muhtemel mutasyonların biriktiği görüldü.
Ekip, ayrıca çıplak kör fare genomunu diğer memelilerle karşılaştırarak, bu canlıda hangi genlerin pozitif seçilime uğradığı, yani evrimsel zaman içinde 'yararlı' mutasyonlar biriktirdiklerini tespit etti. Bu tip 45 gen içinde telomerlerle ilgili iki gen dikkat çekti. Telomerler hücre bölünmesi ve ömrünü belirleyen kromozom yapıları olduğu için, telomerleri etkileyen genlerdeki değişimler de çıplak kör farenin aşırı uzun ömrüne katkıda bulunuyor olabilir. Bu canlıyla yapılan en yeni çalışma da aynı şekilde, hayvanın yüksek karbondioksit bulunan ortamda yaşaması nedeniyle geçirdiği bir mutasyonun iyon kanallarında yarattığı değişikliğin, türün hayatta kalmasını sağladığını göstermiştir.
Yararlanılan ve alıntı yapılan kaynaklar:
-
Lin, E.C.C., & Wu, T.T. (1984) Functional divergence of the L-Fucose system in Escherichia coli. In R.P. Mortlock (ed.), "Microorganisms as Model Systems for Studying Evolution" (pp. 135-164) Plenum, New York.
-
3, 7, 8, 9 ve 10. maddeler Çağrı Yalgın'ın Bilim Güncesi adlı blogunda kaleme aldığı yazısından alıntılar içermektedir.
-
Hartley, B.S. (1984), Experimental evolution of ribitol dehydrogenase. In R.P. Mortlock (ed.), "Microorganisms as Model Systems for Studying Evolution" (pp. 23 - 54) Plenum, New York.
-
Graham Bell’in "Selection - The Mechanism of Evolution" kitabı
-
Kinoshita, et. al., Eur. J. Biochem. 116, 547-551 (1981), FEBS 1981.
-
-
-
-
E. S. J. Smith, D. Omerbasic, S. G. Lechner, G. Anirudhan, L. Lapatsina, G. R. Lewin. The Molecular Basis of Acid Insensitivity in the African Naked Mole-Rat. Science, 2011; 334 (6062): 1557 DOI: 10.1126/science.1213760 Yayın tarihi 16 Aralık 2011.
-
Harun Yahya Safsatası ve Evrim Gerçeği kitabındaki ilgili bölüm, Boğaziçi Ü. Moleküler Biyoloji ve Genetik Bölümü-Mehmet Doğan; Bilim ve Gelecek Kitaplığı (s.214)
-
Drawz, S. M.; Bonomo, R. A. (2010). "Three Decades of β-Lactamase Inhibitors". Clinical Microbiology Reviews, 10.1128/CMR.00037-09.
-
Işın Akyar; Süper Bakteriler İçin Antibiyotik Arayışı, Acıbadem Üniversitesi Sağlık Bilimleri Dergisi. Cilt: 1. Sayı: 2. Nisan 2010.
-
Elena, S. F., V. S. Cooper and R. E. Lenski. 1996. Punctuated evolution caused by selection of rare beneficial mutations. Science 272: 1802-1804.
Şunlar da ilginizi çekebilir: